Фазовое разделениеМатериалы / Теория Брэгга-Вильямса для неидеальных смесей / Фазовое разделение
Для того чтобы жидкости смешивались, необходимо выполнение условия AG < 0. Но этого условия недостаточно для полного смешения жидкостей при любых концентрациях. Изменение свободной энергии при смешении, отнесенное к одному молю, определяется выражением
![]()
На рис. 3 представлены зависимости изменения свободной энергии при смешении ) от мольной доли компонента А для разных значений параметра ч. Верхняя кривая соответствует разделению на фазы при начальной мольной доле 0.5. При этом образуются две фазы, концентрации которых отвечают точкам end.
Уравнение предсказывает, что разделение смеси на фазы происходит всегда прежде всего при условии jca = *в· Разделению смеси на фазы отвечает выполнение условия![]()
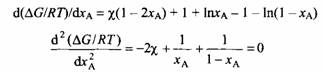
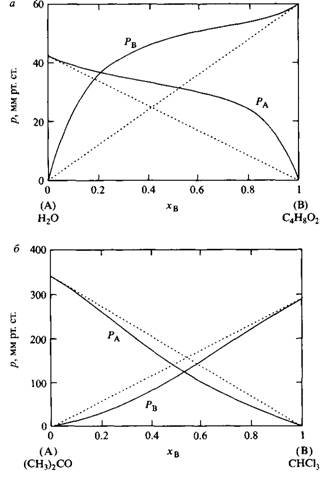
Рис. 2. Вода и диоксан ведут себя как несмешивающиеся жидкости, ацетон и хлороформ, напротив, смешиваются между собой. © 1962 Prentice-Hall Inc., Englewood Cliffs, NJ. С разрешения Pearson Education Limited
Из уравнения следует, что ч = 2 приход*в = 0.5, т. е. разделение смеси на фазы будет происходить при ч > 2. Температура, при которой начинается фазовое разделение, называется критической температурой:
![]()
Теория Брэгга-Вильямса отражает основы физики фазового разделения простых двухкомпонентных систем. Однако известны смеси двух жидкостей, которые полностью смешиваются при низких температурах, но разделяются на фазы при повышении температуры. На рис. 10.4 показаны различные случаи фазового поведения смесей. При повышенных температурах все системы неизбежно обнаруживают верхнюю критическую точку. Это соответствует замкнутой области смешения.
Считается, что нижняя критическая точка связана с влиянием температуры на изменение взаимодействий в смеси Aw. Но эти представления выходят за рамки модели Брэгга-Вильямса и не вносят ничего нового в понимание физического смысла явления. Для систем полиэтиленоксид вода нижняя критическая точка, возможно, появляется вследствие индуцированных температурой структурных изменений оксиэтиленовых групп. Другими словами, для таких систем важную роль играют внутренние степени свободы, что не рассматривает модель Брэгга-Вильямса.
Полезно рассмотреть смешение воды и гидрофобных молекул, например углеводородов. Взаимодействие вода-вода отрицательно и существенно по величине, тогда как взаимодействия вода-углеводород и углеводород-углеводород по сравнению с ww слабые и их можно считать нулевыми. Тогда эффективное парное взаимодействие записывается следующим образом:

Параметр ч для такой системы при комнатной температуре будет иметь значение, близкое к 5. Таким образом, теория Брэгга-Вильямса предсказывает несмешиваемость масла и воды.
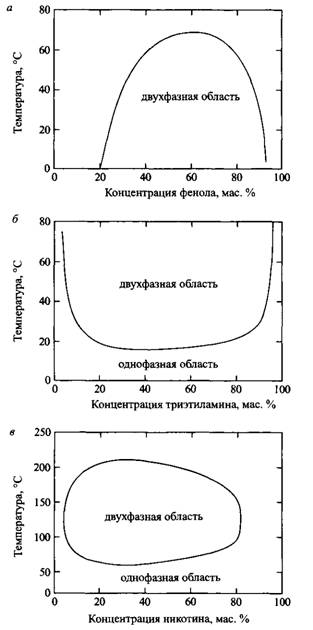
Рис. 3. Фазовые диаграммы смесей с верхними и нижними критическими точками: а — фенол-вода; б — триэтиламин-вода; в — никотин-вода
Теория растворов полимеров Флори-Хаггинса: описание фазовых превращений
Смотрите также
Сырьевая база химического комплекса России
...
Краткая классификация специальных методов ректификационного разделения
...
Заключение
В ходе работы
удалось проследить взаимосвязь между школьными предметами: химией, географией,
физикой, биологией, математикой. Ознакомилась с методами и путями реализации
МПС и опробовала на педагог ...
