Бесконкурентное ингибированиеМатериалы / Ингибирование ферментативной активности / Бесконкурентное ингибирование
В редких случаях степень торможения активности фермента может увеличиваться с повышением концентрации субстрата. Для этого типа торможения был предложен термин "бесконкурентное ингибирование".
Бесконкурентное ингибирование имеет место, когда ингибитор взаимодействует с ферментом только в составе фермент-субстратного комплекса, препятствуя его распаду (Уэбб Л., 1966).
Примером необратимого действия ингибиторов на ферменты могут служить фосфорорганические вещества, применяемые в качестве инсектицидов.
Известно, кроме того, так называемое бесконкурентное ингибирование, когда ингибитор связывается с ферментом также в некаталитическом центре, однако не со свободным ферментом, а только с ES-комплексом в виде тройного комплекса ESI (Т.Т. Березов, Б.Ф. Коровкин, 1990).
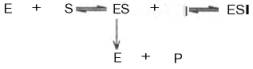
При бесконкурентном ингибировании ингибитор связывается только с фермент-субстратным комплексом, но не со свободным ферментом. Субстрат, связываясь с ферментом, изменяет его конформацию, что делает возможным связывание с ингибитором. Ингибитор, в свою очередь, так меняет конформацию фермента, что катализ становится невозможным
Один из механизмов такого торможения обусловлен возможностью соединения ингибитора с комплексом ES с образованием неактивного или медленно реагирующего тройного комплекса EIS (Т.Т. Березов, Б.Ф. Коровкин, 1990).
Ингибирование субстратом — частный случай бесконкурентного ингибирования, когда две молекулы субстрата связываются с ферментом, что препятствует образованию продукта
Активность многих ферментов тормозится избытком субстрата, причем имеется несколько механизмов этого процесса.
1) Если в образовании фермент-субстратного комплекса участвует несколько функциональных групп фермента, то возможно одновременное присоединение к активному центру двух или более субстратов, что однозначно приведет к образованию неактивного комплекса.
2) В случае избытка субстрата возможно его присоединение не только к активному центру, но и к другим химическим группировкам, функционально связанным с активным центром. Такого рода взаимодействие может помешать ферментативной реакции.
3) Увеличение концентрации субстрата может повысить ионную силу реакционной среды и, как следствие, затормозить скорость ферментативной реакции.
Торможение продуктами реакции связано с тем, что они могут связываться с ферментом или с каким-либо другим компонентом системы таким образом, что скорость прямой реакции снижается.
Смотрите также
Коллоидные системы в организме и их функции
...
Аварийно химически опасные вещества
В соответствие с новым
ГОСТом, переименованы на АХОВ (аварийно химически опасные вещества) Понятия о
АХОВ Растет ассортимент применяемых в промышленности, сельском хозяйстве и быту
химическ ...
Химический анализ силикатов и керамики
Кирпич
является самым древним строительным материалом. В Библии есть упоминание о кирпиче
как о строительном материале уже применительно к временам расселения людей
сразу после Великого Пот ...
